 |
| Terobosan regulasi untuk penyederhanaan standart kriteria, persyaratan dan percepatan pelayanan publik, tanpa mengurangi pengawalan pemenuhan standart manfaat dan mutu. |
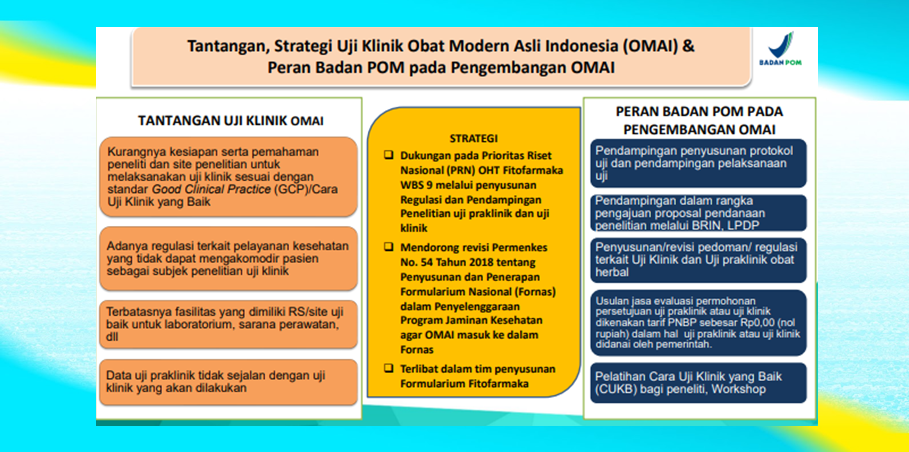
JamuDigital.Com- MEDIA JAMU, NOMOR SATU. Berikut ini Tantangan, Strategi Uji Klinik Obat Modern Asli Indonesia (OMAI) & Peran Badan POM pada Pengembangan OMAI, untuk mengoptimalkan hilirisasi riset herbal untuk menjadi produk komersial yang inovatif.
Tantangan Uji Klinik OMAI:
- Kurangnya kesiapan serta pemahaman peneliti dan site penelitian untuk melaksanakan uji klinik sesuai dengan standar Good Clinical Practice (GCP)/Cara Uji Klinik yang Baik
- Adanya regulasi terkait pelayanan kesehatan yang tidak dapat mengakomodir pasien sebagai subjek penelitian uji klinik
- Terbatasnya fasilitas yang dimiliki RS/site uji baik untuk laboratorium, sarana perawatan, dan lain-lain
- Data uji pra klinik tidak sejalan dengan uji klinik yang akan dilakukan
Strategi Uji Klinik OMAI:
- Dukungan pada Prioritas Riset Nasional (PRN) OHT, Fitofarmaka WBS 9 melalui penyusunan Regulasi dan Pendampingan Penelitian uji pra klinik dan uji klinik
- Mendorong revisi Permenkes No. 54 Tahun 2018 tentang Penyusunan dan Penerapan Formularium Nasional (Fornas) dalam Penyelenggaraan Program Jaminan Kesehatan, agar OMAI masuk ke dalam Fornas
- Terlibat dalam tim penyusunan Formularium Fitofarmaka
Peran Badan POM pada Pengembangan OMAI:
- Pendampingan penyusunan protokol uji dan pendampingan pelaksanaan uji Pendampingan dalam rangka pengajuan proposal pendanaan penelitian melalui BRIN, LPDP
- Penyusunan/revisi pedoman/ regulasi terkait Uji Klinik dan Uji praklinik obat herbal
- Usulan jasa evaluasi permohonan persetujuan uji praklinik atau uji klinik dikenakan tarif PNBP sebesar Rp. 0,00 (nol rupiah) dalam hal uji pra klinik atau uji klinik didanai oleh pemerintah
- Pelatihan Cara Uji Klinik yang Baik (CUKB) bagi peneliti, dan Workshop

Demikian dikemukakan oleh Dra. Dwiana Andayani, Apt, Direktur Registrasi Obat Tradisional, Suplemen Kesehatan Dan Kosmetik, Badan POM saat menyampaikan makalah berjudul "Persetujuan Pelaksanaan Uji Klinik (PPUK) dan Uji Praklinik (PPUPK)" pada Sosialisasi SIAP UK (Sistem Aplikasi Pengajuan Uji Klinik dan Pra Klinik), pada 1 Oktober 2021.
Sementara itu, Deputi Bidang Pengawasan Obat Tradisional, Suplemen Kesehatan, dan Kosmetik Badan POM, Dra. Reri Indriani, Apt., M.Si. dalam sambutannya menjelaskan bahwa terobosan regulasi untuk penyederhanaan standar kriteria dan persyaratan dan percepatan pelayanan publik, tanpa menguragi pengawalan pemenuhan standart manfaat dan mutu. Perlidungan kepada kesehatan masyarakat tetap menjadi yang utama.

"Hilirisasi riset obat herbal menjadi produk komersial dalam rangka untuk kemandirian Indonesia, karena sumber daya Indonesia potensinya luar biasa," Reri Indriani mengingatkan.
Dalam rangka optimalisasi riset dari bahan alam Indonesia, lanjut Reri Indriani, Badan POM meningkatkan pelayanan berbasis digitalisasi. Peran Badan POM menyediakan regulasi, pendampingan dan pembinaan untuk dihilirasi dan dikomersialkan untuk menghasilkan inovasi produk yang bermanfaat untuk masyarakat.
- Berita Terkait: Keunggulan Fraksi Sebagai Bahan Baku Obat Tradisional dan Suplemen
- Berita Terkait: Kriteria Klaim Obat Tradisional Yang Diperbolehkan BPOM
- Berita Terkait: Inovasi Herbal untuk Kemandirian Kesehatan Nasional
Dwiana Andayani juga menjelaskan tentang tupoksi Badan POM yang selaras dengan Inpres No.6/2016 dalam rangka mendukung kemandirian obat nasional.

Uji Klinik adalah kegiatan penelitian yang memiliki nilai ilmiah dan etik dengan mengikutsertakan subjek manusia disertai adanya intervensi produk uji, untuk menemukan atau memastikan efek klinik, farmakologik dan/atau farmakodinamik dan/atau mengidentifikasi reaksi yang tidak diinginkan, atau mempelajari ADME dengan tujuan memastikan keamanan dan efektifitas produk yang diteliti (PerKa Badan Nomor 21 Tahun 2015 tentang Tata Laksana Persetujuan Uji Klinik).
Uji klinik terdiri atas: Uji klinik pra pemasaran: meliputi uji klinik fase I, II, dan III. Uji klinik pasca pemasaran: uji klinik fase IV, Pelaksanaan Uji Klinik: Persetujuan/Notifikasi. Uji klinik pra pemasaran: wajib mendapatkan persetujuan Kepala Badan POM.
Uji klinik pasca pemasaran: wajib menyampaikan notifikasi kepada Kepala Badan POM. Persetujuan Pelaksanaan Uji Klinik (PPUK) yang diberikan oleh Kepala Badan: berlaku 2 (dua) tahun sejak tanggal diterbitkan. Jika pelaksanaan uji klinik melebihi 2 (dua) tahun: dapat diperpanjang dengan alasan yang jelas. Redaksi JamuDigital.Com






















